O que é a IEC 62304?
O IEC 62304 é uma norma harmonizada internacional que fornece orientação ao fabricante sobre o planejamento, desenvolvimento e atividades de vigilância pós-mercado para software de dispositivo médico para garantir que as empresas estejam em conformidade com os requisitos das agencias reguladoras internacional.
A sua primeira versão foi publicada em 2006 e não esclarecia pontos importantes sobre a classificação de segurança de software e implementação desta norma em softwares legados. A emenda 1 de 2015 veio esclarecer principalmente esses pontos. A princípio essa norma estava direcionada era software que integravam equipamentos médicos incluindo os softwares embarcados (firmware), contudo na época o conceito de software como produto médico, ou seja , softwares utilizados com propósitos médicos (SaMD - Software as a Medical Device) , não era conhecido.
A velocidade da evolução de softwares e aplicativos neste período tem encontrado barreiras em seguir essa norma, o que tem atrasado a publicação da versão 2 da norma. Hoje está em discussão a terceira proposta desta versão da norma, que propõe processo de ciclo de vida de software que engloba os software guiados pela atual IEC 62304 e permite a aderência desta novas soluções de software aos requisitos da norma. Mas isso é assunto para outro post. Nesta publicação vou demostrar os principais pontos da norma atual.
Campo de aplicação
A norma IEC 62304 aplica-se ao desenvolvimento e manutenção de software de equipamento médico quando o software é por si só um dispositivo médico ou quando o software é um parte embarcada ou integral do equipamento médico
Esta norma não cobre validação da versão final do equipamento médico.
A conformidade é determinada pela inspeção de todos os documentos obrigatórios norma incluindo o arquivo de gerenciamento de risco, e avaliação dos processos, atividades e tarefas necessárias para a classe de segurança do software.
Classificação de segurança do software
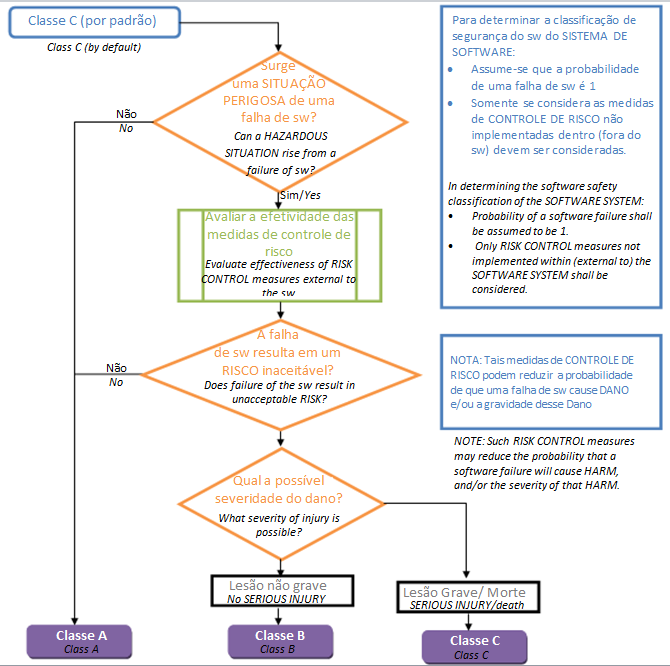
IEC 62304 identifica três classes de segurança para software de dispositivo médico:
Classe A: Nenhum ferimento ou dano à saúde é possível.
Classe B: Lesões são possíveis, mas não são graves.
Classe C: Possibilidade de morte ou ferimentos graves.
Essa classificação ajuda o fabricante a identificar os processos relacionados à segurança necessários ao longo do ciclo de vida do software do dispositivo médico. Os requisitos aplicáveis são específicos para o desenvolvimento e codificação, lançamento e manutenção de software de dispositivos médicos. Eles são codificados nos componentes da IEC 62304.
Composição da IEC 62304
O IEC 62304 para desenvolvimento de software de dispositivo médico delineia os componentes em cinco cláusulas, numeradas de 5 a 9.
Cláusula 5: descreve o processo de desenvolvimento de software, desde o planejamento até o lançamento.
Cláusula 6: descreve a manutenção necessária do software lançado.
Cláusula 7: Especifica o gerenciamento de risco necessário desde a avaliação de falhas até a identificação de riscos potenciais e implementação de recursos para evitá-los.
Cláusula 8: Estabelece os requisitos de gerenciamento de configuração sobre como gerenciar o ambiente de desenvolvimento.
Cláusula 9: Explica os processos de resolução de problemas em relação ao rastreamento e avaliação para resolver os problemas à medida que surgem.
Checklist da IEC 62304:2006 Amd1: 2015
Espero que tenham gostado. Coloque nos comentários se querem aprofundar esse assunto ou sugiram um assunto que gostariam que fosse apresentado para discussão nos posts.
Solicite nos comentários o checklist desta norma,deixe seu nome e e-mail te enviaremos gratuitamente.
Até o próximo post




